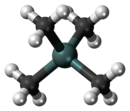
டெட்ராமெத்தில்வெள்ளீயம்
| |||
| பெயர்கள் | |||
|---|---|---|---|
| விருப்பத்தெரிவு ஐயூபிஏசி பெயர்
டெட்ராமெத்தில்சிடானேன்[1] | |||
| வேறு பெயர்கள்
வெள்ளீயம் டெட்ராமெத்தில்
| |||
| இனங்காட்டிகள் | |||
| 594-27-4 | |||
Beilstein Reference
|
3647887 | ||
| ChEBI | CHEBI:30420 | ||
| ChemSpider | 11171 | ||
| EC number | 209-833-6 | ||
Gmelin Reference
|
1938 | ||
| யேமல் -3D படிமங்கள் | Image | ||
| பப்கெம் | 11661 | ||
| வே.ந.வி.ப எண் | WH8630000 | ||
| |||
| UNII | 8V4XU9DPBK | ||
| UN number | 3384 | ||
| பண்புகள் | |||
| C4H12Sn | |||
| வாய்ப்பாட்டு எடை | 178.85 g·mol−1 | ||
| தோற்றம் | நிறமற்ற நீர்மம் | ||
| அடர்த்தி | 1.291 கி செ.மீ−3 | ||
| உருகுநிலை | −54 °C (−65 °F; 219 K) | ||
| கொதிநிலை | 74 முதல் 76 °C (165 முதல் 169 °F; 347 முதல் 349 K) | ||
| தீங்குகள் | |||
| GHS pictograms |   
| ||
| GHS signal word | அபாயம் | ||
| H225, H300, H310, H330, H410 | |||
| P210, P233, P240, P241, P242, P243, P260, P262, P264, P270, P271, P273, P280, P284 | |||
| தீப்பற்றும் வெப்பநிலை | −12 °C (10 °F; 261 K) | ||
மாறுதலாக ஏதும் சொல்லவில்லை என்றால் கொடுக்கப்பட்ட தரவுகள் யாவும் பொருள்கள் அவைகளின் இயல்பான வெப்ப அழுத்த நிலையில் (25°C, 100kPa) இருக்கும். | |||
டெட்ராமெத்தில்வெள்ளீயம் (Tetramethyltin) என்பது (CH3)4Sn என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட கரிம வேதியியல் சேர்மமாகும். ஓர் எளிமையான கரிம உலோகச் சேர்மமான இது நீர்மநிலையில் காணப்படுகிறது. அமில குளோரைடுகளை மெத்தில் கீட்டோன்களாகவும், அரைல் ஆலைடுகளை அரைல் மெத்தில் கீட்டோன்களாகவும் மாற்றும் செயல்முறையில் இச்சேற்மம் பயனுள்ளதாக இருக்கும். எளிதில் ஆவியாகும் என்பதாலும் நச்சுத்தன்மை வாய்ந்தது என்பதாலும் இதை ஆய்வகத்தில் பயன்படுத்தும் போது கவனமாக இருக்க வேண்டும்.
தயாரிப்பு
[தொகு]வெள்ளீயம் டெட்ராகுளோரைடுடன் கிரிக்னார்டு வினையாக்கியான மெத்தில்மக்னீசியம் அயோடைடைச் சேர்த்து வினை புரியச் செய்வதால் டெட்ராமெத்தில்வெள்ளீயம் உருவாகிறது.[2] குளோரின் வாயுவுடன் வெள்ளீயம் உலோகத்தைச் சேர்த்து வினைபுரியச் செய்து வெள்ளீயம் டெட்ராகுளோரைடு தயாரித்துக் கொள்ளப்படுகிறது.[3]
- 4 CH3MgI + SnCl4 → (CH3)4Sn + 4 MgICl
கட்டமைப்பு
[தொகு]டெட்ராமெதில்வெள்ளீயத்தில் நான்கு மெத்தில் குழுக்களால் சூழப்பட்ட உலோகம் ஒரு நான்முகி அமைப்பில் நியோபெண்டேன் கட்டமைப்பை ஒத்துள்ளது.
பயன்பாடுகள்
[தொகு]மெத்தில்வெள்ளீய சேர்மங்களின் முன்னோடி
[தொகு]டெட்ராமெத்தில்வெள்ளீயம் சேர்மம் மும்மெத்தில்வெள்ளீயக் குளோரைடு மற்றும் தொடர்புடைய மெத்தில்வெள்ளீயம் ஆலைடு சேர்மங்கள் தயாரிப்பதற்கு உதவும் ஒரு முன்னோடிச் சேர்மமாகும். இவை பிற கரிமவெள்ளீயச் சேர்மங்கள் தயாரிக்க உதவும் முன்னோடிகளாக உள்ளன. இந்த மெத்தில்வெள்ளீயக் குளோரைடுகள் கோசெசுகோவ் மறுபகிர்வு வினை மூலம் தயாரிக்கப்படுகின்றன. இவ்வாறு, (CH3)4Sn மற்றும் SnCl4 ஆகியவை 100 °செல்சியசு மற்றும் 200 °செல்சியசு வெப்பநிலைகளுக்கு இடையேயான வெப்பநிலையில் வினைபுரிந்து (CH3)3SnCl சேர்மத்தை ஒரு விளைபொருளாகக் கொடுக்கின்றன.
- SnCl4 + 3 (CH3)4Sn → 4 (CH3)3SnCl
டெட்ராமெத்தில்வெள்ளீயத்தைப் பயன்படுத்தி மும்மெத்தில்வெள்ளீயக் குளோரைடு தயாரிப்பதற்கான இரண்டாவது வழி பாதரச(II) குளோரைடை டெட்ராமெத்தில்வெள்ளீயத்துடன் சேர்த்து வினைபுரியச் செய்வதாகும்.[2]
- 4 HgCl2 + 4 (CH3)4Sn → 4 Me3SnCl + 4 MeHgCl
பல்வேறு வகையான மெத்தில்வெள்ளீய சேர்மங்கள் பாலிவினைல் குளோரைடு நிலைப்படுத்திகளுக்கு முன்னோடிகளாகப் பயன்படுத்தப்படுகின்றன[3]
மேற்பரப்பு செயல்பாடு
[தொகு]டெட்ராமெதில்வெள்ளீயம் வாயு நிலையில் சுமார் 277 ° செல்சியசு வெப்பநிலையில் சிதைகிறது; (CH3)4Sn ஆவி சிலிக்காவுடன் வினைபுரிந்து (CH3)3Sn-ஒட்டுதல் திடப்பொருளைக் கொடுக்கிறது.
- (CH3)4Sn + ≡SiOH → ≡SiOSn(CH3)3 + MeH
இந்த வினை மற்ற அல்கைல் பதிலீடுகளாலும் கூட சாத்தியமாகும். இதேபோன்ற ஒரு செயல்பாட்டில், டெட்ராமெதில்வெள்ளீயம் சில சியோலைட்டுகளை −90 °செல்சியசு வெப்பநிலை வரையிலான குறைந்த வெப்பநிலையில் செயல்பட பயன்படுத்தப்படுகிறது.[4]
கரிமத்தொகுப்பு வினைகளில் =
[தொகு]கரிமத் தொகுப்பு வினைகளில் டெட்ராமெதில்வெள்ளீயம் அமில குளோரைடுகளுடன் பல்லேடியம்-வினையூக்க பிணைப்பு வினைகளுக்கு உட்பட்டு மெத்தில் கீட்டோன்களை அளிக்கிறது.:[5]
- SnMe4 + RCOCl → RCOMe + Me3SnCl
மேற்கோள்கள்
[தொகு]- ↑ "Tetramethyltin | C4H12Sn". ChemSpider. பார்க்கப்பட்ட நாள் 2013-09-15.
- ↑ 2.0 2.1 Scott, W. J.; Jones, J. H.; Moretto, A. F. (2002). "Tetramethylstannane". Encyclopedia of Reagents for Organic Synthesis. doi:10.1002/047084289X.rt070. பன்னாட்டுத் தரப்புத்தக எண்:0471936235.
- ↑ 3.0 3.1 Thoonen, S. H. L.; Deelman, B.; van Koten, G (2004). "Synthetic Aspects of Tetraorganotins and Organotin(IV) Halides". Journal of Organometallic Chemistry 689 (13): 2145–2157. doi:10.1016/j.jorganchem.2004.03.027.
- ↑ Davies, A. G. (2008). "Tin Organometallics". In Robert H. Crabtree; D. Michael P. Mingos (eds.). Comprehensive Organometallic Chemistry III. Elsevier. pp. 809–883. எண்ணிம ஆவணச் சுட்டி:10.1016/B0-08-045047-4/00054-6. பன்னாட்டுத் தரப்புத்தக எண் 9780080450476.
- ↑ Labadie, J.; Stille, J. (1983). "Mechanisms of the palladium-catalyzed couplings of acid chlorides with organotin reagents". J. Am. Chem. Soc. 105 (19): 6129. doi:10.1021/ja00357a026.